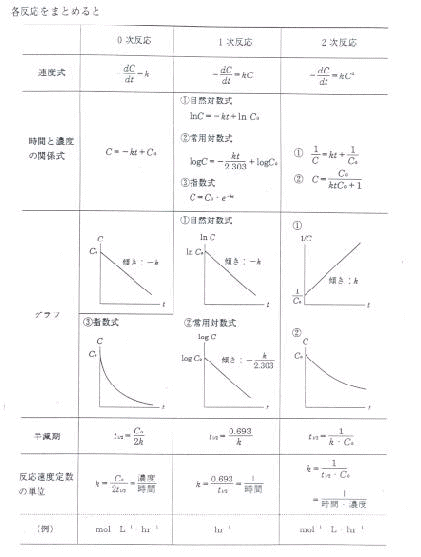
問 19 物質Aの濃度が減少するとき、その反応速度は一般に次式で示される。
-d[A]/dt=k[A]n
nは反応次数、kは反応速度定数、tは時間である。また、[A]0を初期濃度と
するとき、反応次数(n)と積分反応速度式との関係は次のように示される。
反応次数(n)積分反応速度式
a 0 [A]=[A] 0-kt
b 1 ln[A]=ln[A] 0-kt
c 2 [A]-1=kt+[A] 0-1
反応速度定数kの次元について、正しい組合せはどれか。
a b c
1 時間-1-時間-1-時間-1
2 濃度・時間-1-時間-1-濃度・時間-1
3 濃度-濃度-1・時間 -1-濃度-1
4 濃度・時間-1-時間-1-濃度-1・時間-1
5 濃度-1-濃度・時間-1-濃度-1
_
解答 4
この問題では、上に与えられた式をK=の形に変形すれば簡単である。
a k=([A]0-[A])/t=濃度/時間
b k=(ln[A]0-ln[A])/t=1/時間
c k=1/([A]0-[A])・t=1/濃度・時間
