Our RESEARCH
研究テーマ
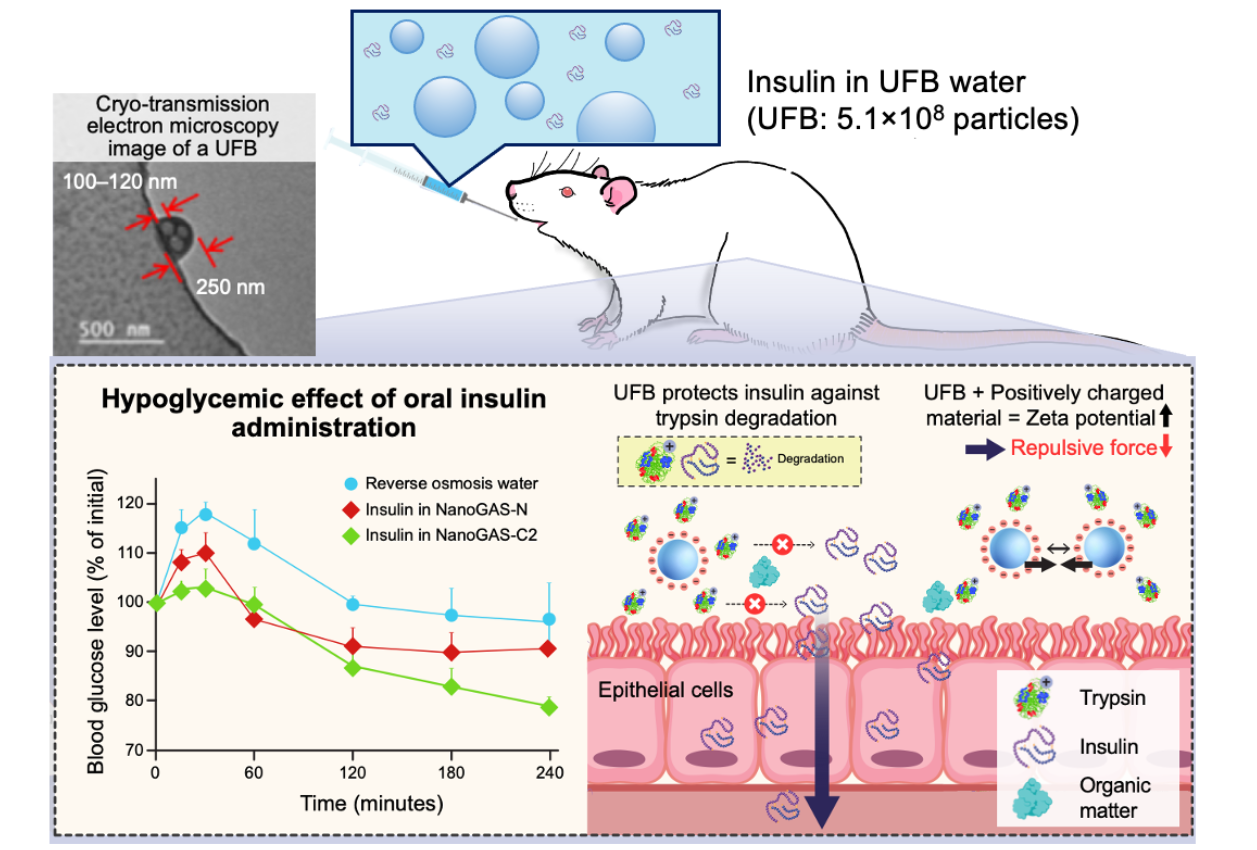
ウルトラファインバブルの医療分野への応用
「ウルトラファインバブル (UFB)」は、表面が負に帯電した1μm未満の微細な泡です。当研究室ではこのUFBの特性に着目し、医療分野における活用法を探索しています。これまでに、UFBが生体適合性の高い素材であり、生理活性化作用をもつ気体を封入して経口摂取によって生体組織に送達できることを明らかとしました。さらに、UFBとともにバイオ医薬(インスリン)を経口投与することにより、腸粘膜における吸収が増大し、注射以外の経路でも薬理作用(血糖値調節)を発揮できるようになることを見出しました。この発見をもとに、現在はUFBを医療に貢献する多機能素材として活用し、薬物・気体送達キャリアとして社会実装につなげることを目指しています。
Morishita et al., 2025, Biol. Pharm. Bull. 48, 1594-1602.
Morishita et al., 2025, Int. J. Pharm. 673, 125378.
Morishita et al., 2024, Biol. Pharm. Bull. 47, 1106-1112.
Morishita et al., 2023, Biol. Pharm. Bull. 46, 343-347.
Morishita et al., 2022, Biocontrol. Sci. 27, 139-142.
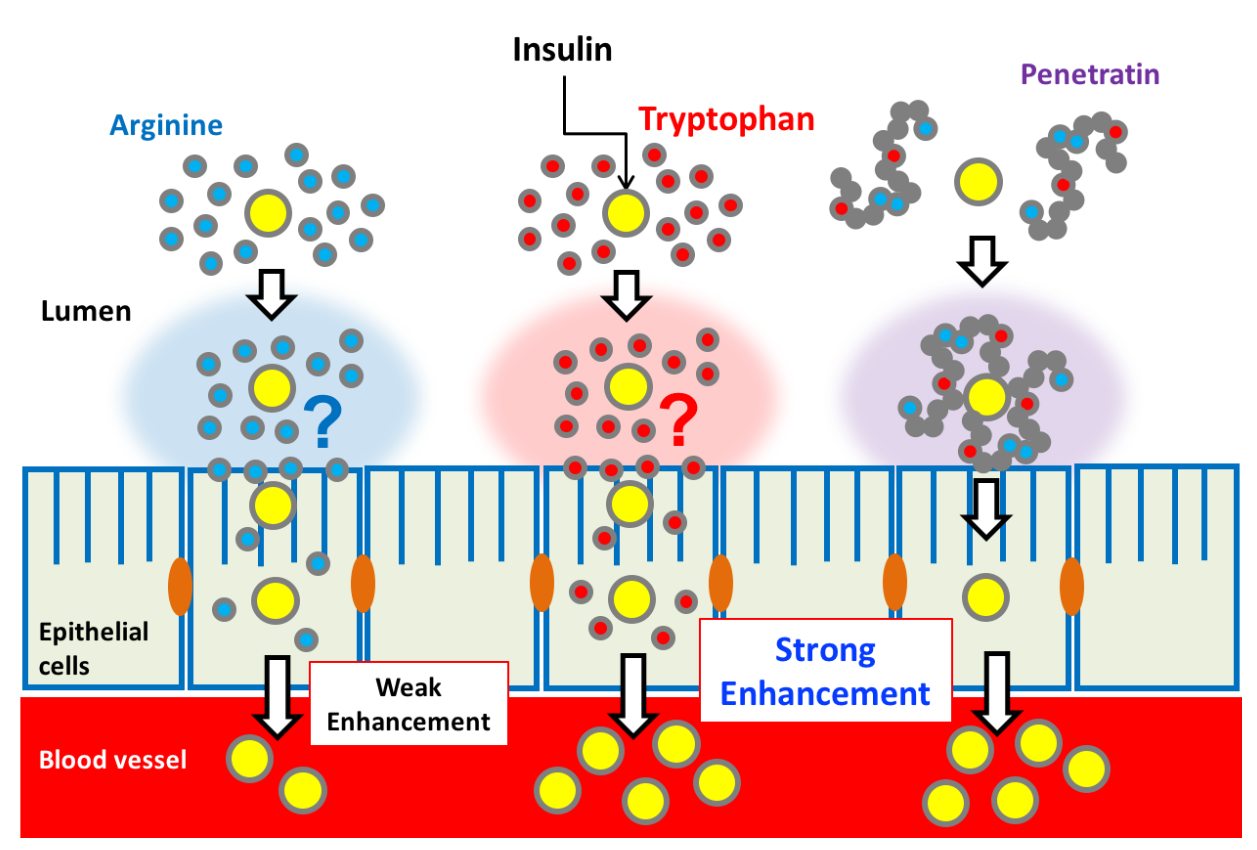
バイオ医薬品の経口・経鼻デリバリー法の開発
米国・テキサス大学と共同開発したスマートハイドロゲル粒子、また最近では、細胞膜透過ペプチド(cell-penetrating peptides)に着目し、これらがインスリン、カルシトニン、インターフェロンあるいはワクチンなど、バイオ薬物の有効かつ安全な経粘膜吸収促進キャリアシステムになることを世界で初めて見出しました。また、これらDDSキャリアの生体への安全性を理化学研究所との共同研究で、PETイメージング手法を用いて可視化することに成功しました。さらに最近では、単独のアミノ酸(アルギニン、トリプトファン)がバイオ薬物の経口吸収キャリアになることを発見しました。現在、cell-penetrating peptidesやアミノ酸を用いたバイオ薬物の経口・経鼻投与製剤の実用化に向け、研究を進めています。
Itagaki et al., 2023, J. Pharm. Sci. 112, 2591-2595.
Kamei et al., 2020, Eur. J. Pharm. Biopharm. 155, 77-87.
Kamei et al., 2020, Pharm. Res. 37, 182.
Kamei et al., 2018, Pharmaceutics 10, 182.
Fukuoka et al., 2018, Biol. Pharm. Bull. 41, 811-814.
Kamei et al., 2018, Biol. Pharm. Bull. 41, 239-246.
Kamei et al., 2017, Int. J. Pharm. 521, 176-183.
Yoshida et al., 2017, Eur. J. Pharm. Biopharm. 112, 138-142.
Iwase et al., 2016, Int. J. Pharm. 510, 304-310.
Muto et al., 2016, J. Pharm. Sci. 105, 2014-2017.
Kamei et al., 2016, J. Pharm. Sci. 105, 747-753.
Khafagy et al., 2015, AAPS J. 17, 1427-1437.
Kamei et al., 2015, Eur. J. Pharm. Biopharm. 94, 42-51.
Nielsen et al., 2015, Biol. Pharm. Bull. 38, 144-146.
Nielsen et al., 2014, J. Control. Release 189, 19-24.
Khafagy et al., 2013, Eur. J. Pharm. Biopharm. 85, 736-743.
Kamei et al., 2013, J. Pharm. Sci. 102, 3998-4008.
Kamei et al., 2013, J. Pharm. Sci. 102, 469-479.
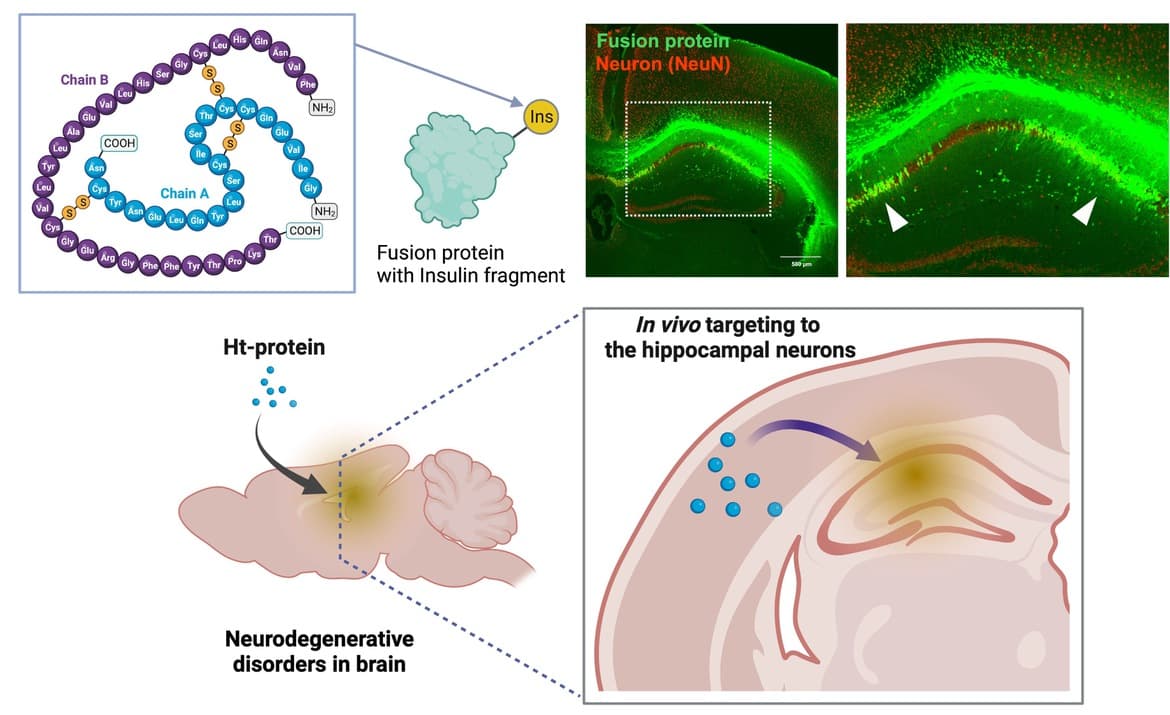
インスリンの融合・修飾に基づく海馬への薬物標的化
近年、当研究室では経鼻投与を介して脳に到達したインスリンが海馬の神経細胞層に特異的に集積しうることを見出しました。このインスリンの性質を薬物送達キャリアとして応用することにより、他の薬物(タンパク質・核酸医薬)を海馬神経細胞へと効率的に集積させることが可能になると考えました。本技術を、認知症などの神経変性疾患治療薬の開発促進に活用することを目指しています。また、細胞外小胞キャリアと組み合わせたDDSの開発も進めています。
Kamei et al., 2025 Expert Opin Drug Deliv 22, 1807-1810.
Kamei et al., 2024, PNAS 121, e2407936121.
Kamei et al., 2021, Nanomedicine 35, 102396
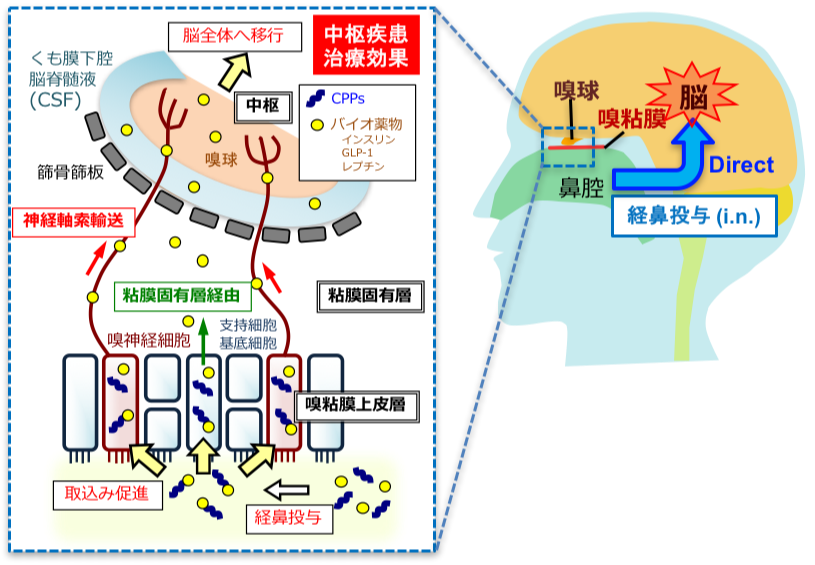
経鼻投与法を介したバイオ医薬品の脳デリバリー
近年、経鼻ルートを介した脳へのドラッグデリバリーが注目されています。血液脳関門を介さずに、しかも非侵襲的に脳への薬物送達を可能にするルートとして期待されています。しかし、タンパクやペプチドなどの高分子生理活性バイオ医薬品については、鼻から脳への移行効率が十分ではありません。当研究室ではcell-penetrating peptides等の粘膜透過促進手法を利用して、嗅神経細胞や嗅粘膜上皮細胞への薬物の取込みを向上させることを試みています。本研究に基づき、中枢疾患バイオ医薬品の非侵襲的かつ効率的なデリバリー技術の構築を目指しています。
Kamei et al., 2022, Drug Deliv. Transl. Res. 12, 2667-2677.
Kamei et al., 2021, Pharmaceutics 13, 1745.
Khafagy et al., 2020, J. Control. Release 319, 397-406.
Kamei et al., 2018, Sci. Rep. 8, 17641.
Kamei et al., 2018, Biol. Pharm. Bull. 41, 546-554.
Kamei et al., 2017, Mol. Pharm. 14, 916-927.
Kamei et al., 2016, Mol. Pharm. 13, 1004-1011.
Kamei and Takeda-Morishita, 2015, J. Control. Release197, 105-110.
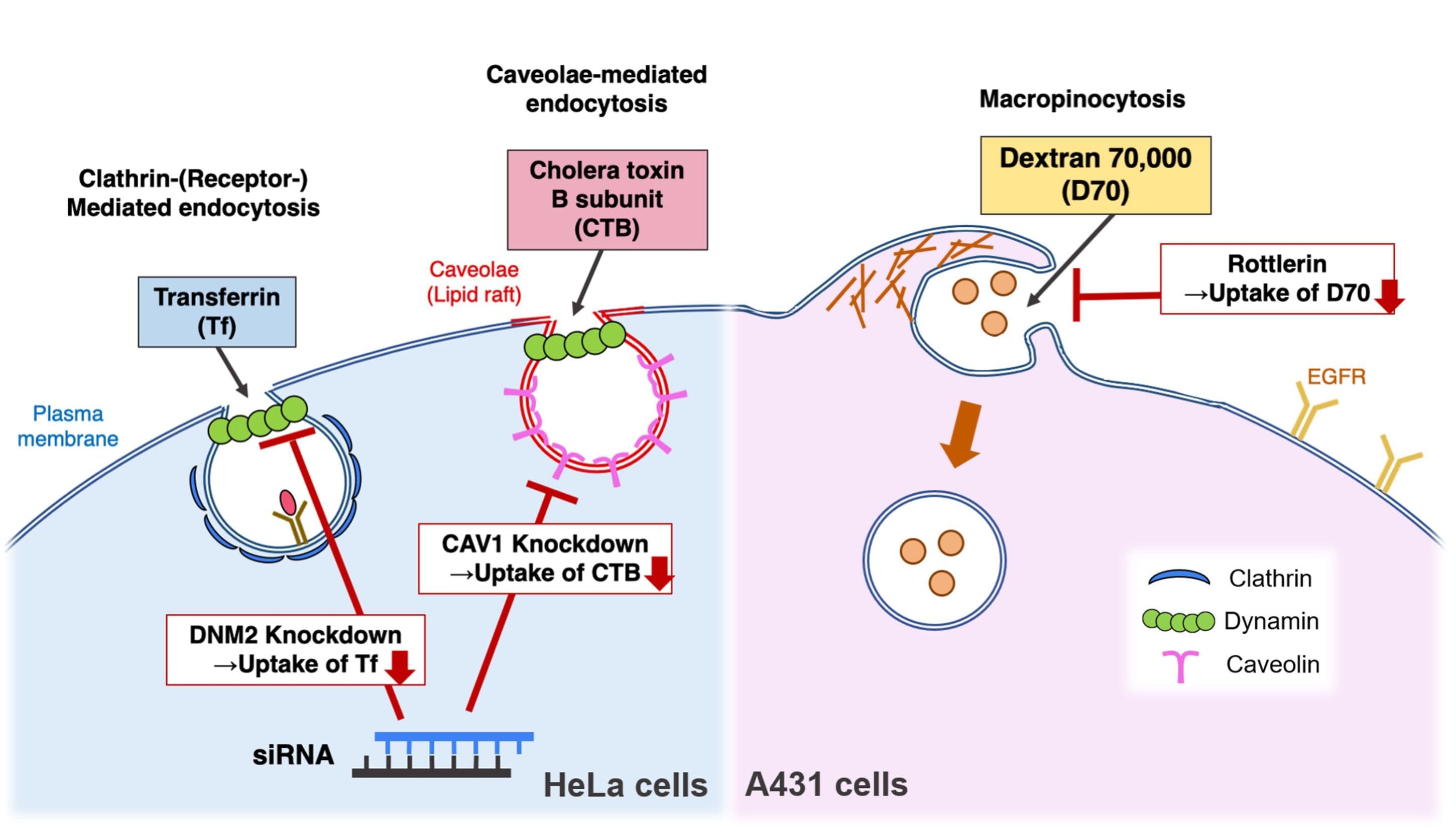
DDSキャリアの細胞内移行メカニズムの解析
薬物が目的組織に到達するためには、種々の生体膜を透過しなければなりません。特に、近年注目されるタンパク質薬物や核酸治療薬は、細胞質や核といった細胞の内部で効果を発揮するものが多いため、ナノ粒子キャリアや細胞内導入ツール等のDDS技術を使って効果的にそれらの薬物を細胞内に送達することが求められます。考案したDDS技術が有用であるか、また、生体にとって安全かどうかを見極めるためには、そのメカニズムを明らかにする必要があります。本研究室では、DDSキャリアの細胞内移行メカニズムを正確に評価するための手法を確立することを目指しています。
Itagaki and Kamei, 2025, FEBS Lett. 599, 1509-1517.
Itagaki et al., 2023, FASEB J 37, e22764.
Kamei et al., 2019, J. Control. Release 310, 127-140
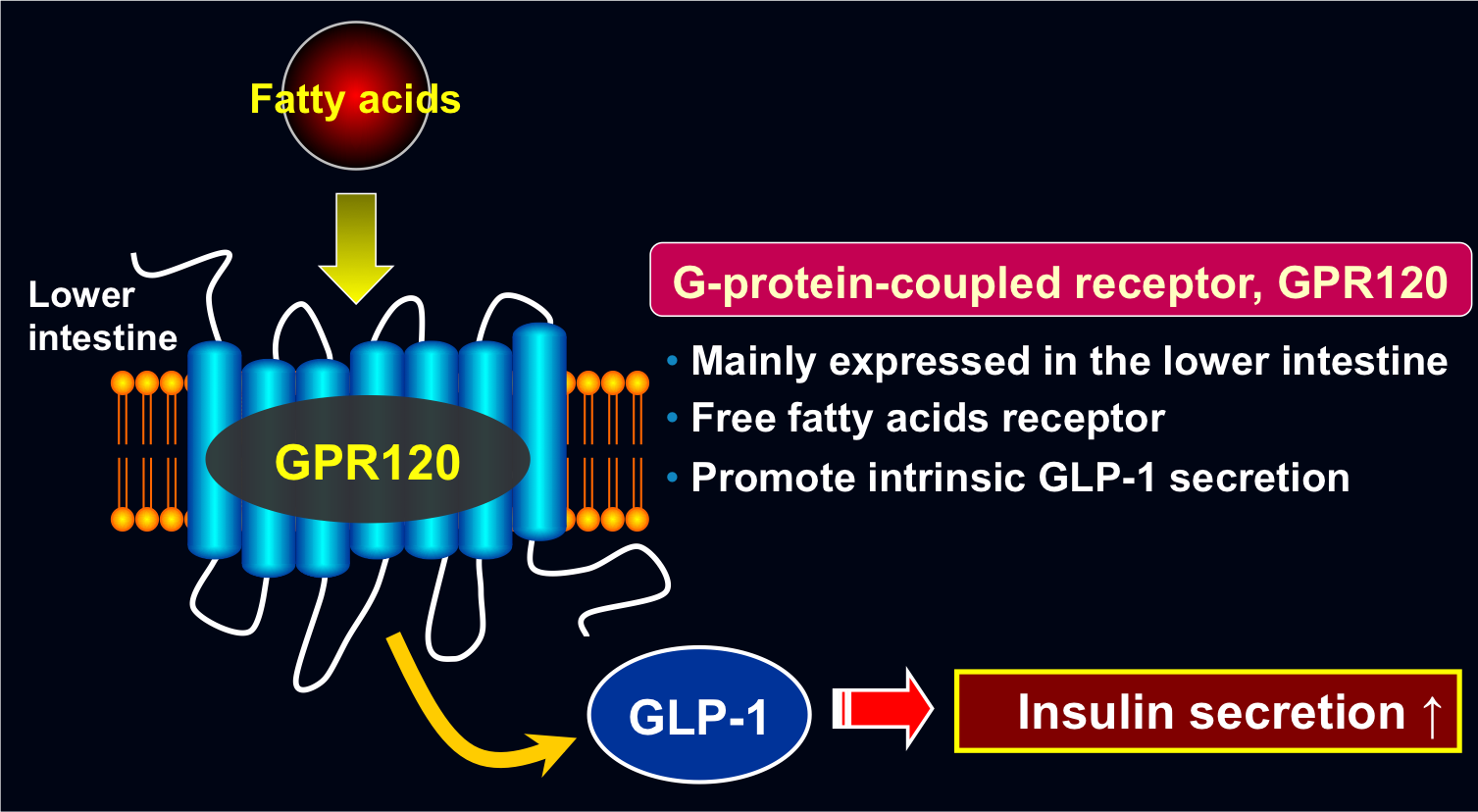
高度不飽和脂肪酸を利用した新規糖尿病治療法の開発
魚由来成分であるドコサヘキサエン酸 (DHA) やエイコサペンタエン酸 (EPA) は、従来から健康食品やサプリメントとして広く用いられています。近年当研究室では、これらの高度不飽和脂肪酸が結腸に発現する受容体を刺激し、インクレチンホルモンの一種であるグルカゴン様ペプチド (GLP-1) の分泌促進作用・血糖降下作用を示すことを明らかにしました。さらに糖尿病モデルマウスの結腸へのDHA長期投与は、病態時における膵島過形成を抑制し、これが血糖改善に寄与する可能性も示してきました。より効果的なDHA・EPAの投与剤形や結腸デリバリー手法を構築し、安全かつ有効な新規糖尿病治療法の実現を目指している。
Iwase et al., 2016, Jpn. J. Pharm. Diabetes 5, 180-187.
Shida et al., 2013, Int. J. Pharm. 450, 63-69.
Tanaka et al., 2008, J. Control. Release 132, 99-104.

